Tóm Tắt
1. Nguyên tử khối là gì?
1.1. Đơn vị khối lượng nguyên tử là gì?
Đơn vị Cacbon là đơn vị sử dụng để đo khối lượng nguyên tử, có ký hiệu là đvC. Một đơn vị Cacbon bằng 1/12 của khối lượng hạt nhân nguyên tử Cacbon đồng vị C12.
Bạn đang đọc: Cách Tính Nguyên Tử Khối – Cách Để Tính Nguyên Tử Khối
Do nguyên tử Cacbon đồng vị C12 phổ cập cùng với đố là chỉ số sai là rất thấp nên Viện thống kê giám sát Quốc tế đã thống nhất dùng đơn vị chức năng Cacbon này .
1.2. Vậy nguyên tử khối là gì?
Nguyên tử khối có thể được hiểu là khối lượng tương đốicủa một nguyên tử có đơn vị tính là đơn vị cacbon (ký hiệu đvC). Mỗi nguyên tố có số lượng proton và notron khác nhau nên sẽ có nguyên tử khối khác nhau.
Nguyên tử khối của một nguyên tử là khối lượng tương đối của nguyên tử nguyên tố, là tổng khối lượng notron, proton và electron nhưng do khối lượng của electron nhỏ nên sẽ không tính khối lượng này. Do đó, nguyên tử khối xấp xỉ bằng khối của hạt nhân.
Nguyên tử khối cũng được xem là khối lượng, được tính theo đơn vị gam của một mol nguyên tử, ký hiệu bằng u.
1 u = 1 / NA gam = 1 / ( 1000N a ) kg
Trong đó Na chính là hàng số Avogadro
1 u xấp xỉ bằng 1.66053886 x 10-27 kg
1 u xấp xỉ bằng 1.6605 x 10-24 g
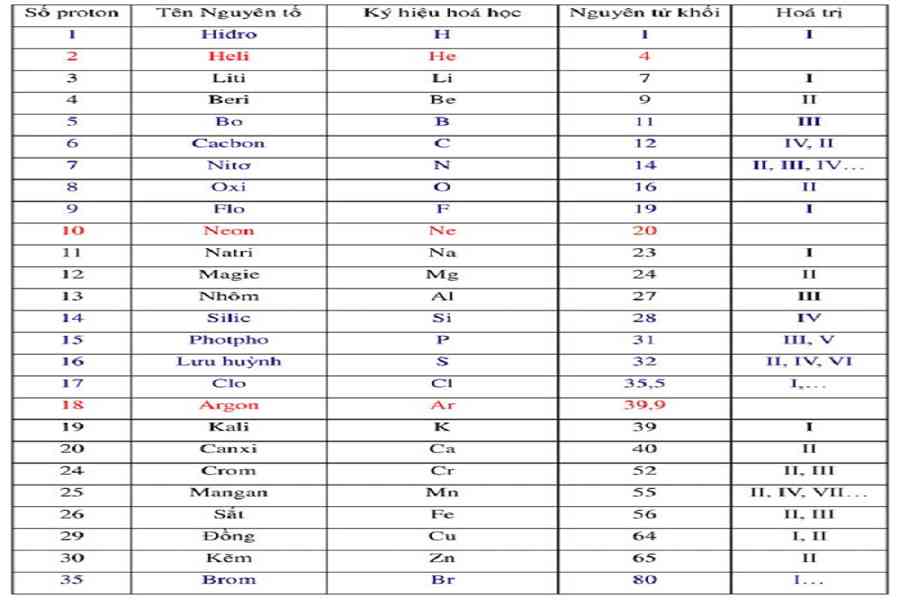
| Số p |
Tên nguyên tố |
Ký hiệu hoá học | Nguyên tử khối |
Hoá trị
|
| 1 |
Nguyên tử khối của Hiđro |
H | 1 | I |
| 2 | Nguyên tử khối của Heli | He | 4 | |
| 3 | Nguyên tử khối của Liti | Li | 7 | I |
| 4 | Nguyên tử khối của Beri | Be | 9 | II |
| 5 | Nguyên tử khối của Bo | B | 11 | III |
| 6 | Nguyên tử khối của Cacbon | C | 12 | IV, II |
| 7 | Nguyên tử khối của Nitơ | N | 14 | III,II,IV,.. |
| 8 | Nguyên tử khối của Oxi | O | 16 | II |
| 9 | Nguyên tử khối của Flo | F | 19 | I |
| 10 | Nguyên tử khối của Neon | Ne | 20 | |
| 11 | Nguyên tử khối của Natri | Na | 23 | I |
| 12 | Nguyên tử khối của Mg(Magie) | Mg | 24 | II |
| 13 | Nguyên tử khối của Nhôm | Al | 27 | III |
| 14 | Nguyên tử khối của Silic | Si | 28 | IV |
| 15 | Nguyên tử khối của Photpho | P | 31 | III, V |
| 16 | Nguyên tử khối của Lưu huỳnh | S | 32 | II,IV,VI,.. |
| 17 | Nguyên tử khối của Clo | Cl | 35,5 | I,.. |
| 18 | Nguyên tử khối của Agon | Ar | 39,9 | |
| 19 | Nguyên tử khối của Kali | K | 39 | I |
| 20 | Nguyên tử khối của Canxi | Ca | 40 | II |
| 24 | Nguyên tử khối của Crom | Cr | 52 | II,III |
| 25 | Nguyên tử khối của Mangan | Mn | 55 | II,IV,VII,..Xem thêm : Cách Tăng Người Theo Dõi Trên Facebook Đơn Giản, Cách Tăng Lượt Theo Dõi Thật Trên Facebook |
| 26 | Nguyên tử khối của Sắt | Fe | 56 | II,III |
| 29 | Nguyên tử khối của Đồng | Cu | 64 | I,II |
| 30 | Nguyên tử khối của Kẽm | Zn | 65 | II |
| 35 | Nguyên tử khối của Brom | Br | 80 | I,… |
| 47 | Nguyên tử khối của Ag (Bạc) | Ag | 108 | I |
| 56 | Nguyên tử khối của Bari | Ba | 137 | II |
| 80 | Nguyên tử khối của Thuỷ ngân | Hg | 201 | I,II |
| 82 | Nguyên tử khối của Chì | Pb | 207 | II,IV |
1.3 Vậy nguyên tử khối có phải số khối không?
Số khối hay số hạt có kí hiệu A là tổng số hạt trong hạt nhân nguyên tử.Số khốiđược tính theo công thức A = Z + N với Z là số proton, N là số neutron. Như vậy ta có thể thấy nguyên tử khối là khối lượng tương đối của một nguyên tử, còn số khối thì là số hạt trong hạt nhân nguyên tử, đây là 2 khái niệm hoàn toán khác nhau.
2. Cách học thuộc bảng nguyên tử khối
Giống như khi mới học bảng tính tantrong hóa học,với bảng nguyên tử khốicác bạn sẽ gặp rất nhiều khó khăn để nhớ rõ nguyên tử khối của từng nguyên tố một. Hầu như trong các bài tập hóa học ở bậc phổ thông, nguyên tử khối đều được cho sẵn ở đầu bài. Tuy nhiên, việc ghi nhớ bảng này là điều vô cùng cần thiết để có thể sử dụng ngay khi cần thiết, đặc biệt là trong những bài toán hóa học áp dụng định luật bảo toàn khối lượng sau này. Vậy làm thế nào để nhớ được nguyên tử khối của Brom, nguyên tử khối Ag hay nguyên tử khối của các nguyên tốc khác?Dưới đây, tôi xin trình bày một số phương pháp để có thể học bảng này một cách nhanh nhất.
2.1. Thường xuyên làm bài tập hóa học
Hóa học là một môn học rất phong phú về bài tập và yên cầu người học luôn luôn phải chịu khó, đào sâu tâm lý. Như đã đề cập ở trên, khi mới làm quen với môn học, nguyên tử khối của từng nguyên tố sẽ được cho sẵn ở đầu bài. Thường xuyên tiếp xúc sẽ giúp bạn nhớ bảng nguyên tử khối một cách rất nhanh mà không cần phải “ học vẹt ” .
2.2. Học qua bài ca nguyên tử khối
Đây là một trong những cách học bảng nguyên tử khối khá phổ biến. Các thầy cô và rất nhiều thế hệ học sinh đi trước đã sáng tác một số bài thơ về khối lượng nguyên tố khá dễ nhớ. Việc của bạn là sưu tầm và học thuộc chúng. Đối với cách học này rất ít khi bạn bị nhầm nguyên tử khối của các nguyên tố với nhau. Hơn nữa, thời gian học cũng được rút ngắn một cách đáng kể.

Bảng nguyên tử khối chuẩn nhấtDo có vần điệu, những bài thơ này rất thuận tiện đi vào bộ nhớ của các bạn. Môn hóa học cũng do đó mà trở nên lí thú và bớt khô khan hơn. Thay vì viết đi viết lại nhiều lần để học thuộc bảng nguyên tử khối, bạn hoàn toàn có thể nhẩm lại một vài bài thơ về yếu tố này. Tin tôi đi, bảo vệ một thời hạn ngắn, bạn sẽ thuộc làu tổng thể các khối lượng của các nguyên tố một cách thuận tiện. Những vần thơ kiểu như đoạn ngắn dưới đây sẽ giúp cho bạn có những khoảng thời gian ngắn học hóa học rất mê hoặc :Hidro số 1 bạn ơiLiti số 7 nhớ ngay thuận tiệnCacbon thì nhớ 12Nito 14 bạn thời chớ quênOxy 16 trăng lênFlo 19 vấn vương riêng sầu
Hay bài:
Hidro là 112 cột CacbonNitơ 14 trònOxi trăng 16Natri hay láu táuNhảy tót lên 23Khiến Magie gần nhàNgậm ngùi nhận 2427 nhôm la lớnLưu huỳnh giành 32Khác người thật là tàiClo 35 rưỡi ( 35,5 )Kali thích 39Canxi tiếp 40
55 Mangan cười
Sắt đây rồi 5664 đồng nổi cáuvì kém kẽm 6580 brom nằmxa bạc 108Bari thì chán ngán137 ích chiKém người ta còn gìThuỷ ngân 201Còn lại chì một cột207 thật toHeli thì buồn soMình đây được có 4Liti thật nhã nhặnSố 7 là được rồiSố 9 Beri ngồiTrêu bạn Bo 1119 đây chết ngộtFlo đang than phiềnNêon thì cười hiềnTớ 20 tròn chẵnSilic người đứng đắnNhận 28 đẹp koPhotpho đỏ hồng hồngNhận 31 cuối thángAgon cười trong sáng39,9 đâyKết thúc bài ca nàyCrom 52 đấyNgoài ra có rất nhiều các bài thơ khác về bảng nguyên tử khối được các thầy cô sáng tác, vần điệu khá đơn thuần, dễ học. Các bạn hoàn toàn có thể tìm hiểu thêm hoặc tìm kiếm thêm trên mạng Internet những bài thơ về nguyên tử khối để quy trình học hóa trở nên bớt căng thẳng mệt mỏi và thuận tiện hơn .
3. Một số ứng dụng của bảng nguyên tử khối trong các bài tập hóa học
Bảng nguyên tử khối có tính ứng dụng rất cao trong môn hóa học, đặc biệt ở phần hóa vô cơ. Hầu hết các bài tập hóa học đều phải áp dụng bảng này. Dưới đây, tôi xin trình bày một số dạng bài cơ bản nhất cần áp dụng trực tiếp bảng phân tử khối tại bậc trung học cơ sở.
3.1. Tìm nguyên tốtrong hợp chất
Đối với những bước tiên phong làm quen với môn hóa học, đây là một trong những dạng bài thông dụng nhất. Dưới đây là một ví dụ minh họa đơn thuần :Hợp chất của sắt kẽm kim loại A phối hợp với axit \ ( H_2SO_4 \ ) tạo ra muối có công thức là \ ( ASO_4 \ ). Tổng phân tử khốicủa hợp chất này là 160 đvC. Xác định nguyên tố A .Ta hoàn toàn có thể thuận tiện giải bài toán này như sau :Trên bảng nguyên tử khối ta thấyNguyên tử khối của S là : 32Nguyên tử khối của oxy là : 16Theo công thức hợp chất ta có A + 32 + 16×4 = 160
3.2. Tìm nguyên tố khi biết nguyên tử khối
Đối với bài tập trắc nghiệm đơn thuần ở lớp 8, các bạn tiếp tục phát hiện 1 số ít câu hỏi nhưXác định nguyên tố có nguyên tử khối gấp 2 lần oxy
Để làm được bài tập này, bạn cần nắm được nguyên tử khối của oxy là 16, nguyên tố có nguyên tử khối gấp 2 lần oxy có nguyên tử khối là 32. Dễ dàng nhận thấy, đáp số của câu hỏi là lưu huỳnh.
Xem thêm: Học Excel – Bài 10: Cách sử dụng Data Validation trong Excel – Trường THPT Thành Phố Sóc Trăng
Các dạng bài tập được nêu trên là một trong những dạng cơ bản và đơn thuần nhất của hóa học bậc trung học. Tuy nhiên, trước khi đi vào tìm hiểu và khám phá sâu hơn về hóa, ta cũng cần phải nắm được các kỹ năng và kiến thức cơ bản nhất để có một khởi đầu thuận tiện và một nền tảng thật chắc như đinh bạn nhé .
Hóa học là một trong những môn học quan trọng không chỉ tại trường học mà còn trong thực tế. Để học tốt môn học này đòi hỏi bạn cần phải có phương pháp học cũng như nền tảng kiến thức thật chắc chắn. Chìa khóa để chinh phục môn học này nằm ở chính bản thân các bạn. Nếu thiếu ý chí quyết tâm và tinh thần ham học hỏi thì dù có áp dụng phương pháp nào, bạn cũng khó mà tiếp thu được các kiến thức hóa học, dù là đơn giản nhất. Các bạn cũng có thể tìm gia sư học cùng để giúp mình tiến bộ nhanh hơn hay đơn giản là kiếm một người bạn học tốt môn hóa học nhóm.
Trên đây là một số ít điều cơ bản về bảng nguyên tử khối trong hóa học. Hi vọng hoàn toàn có thể giúp các bạn trong những bước tiên phong làm quen với môn học này. Chúc bạn thành công xuất sắc trong môn hóa nói riêng và trong hàng loạt quy trình học tập nói chung !
Source: https://final-blade.com
Category: Kiến thức Internet